Diese Packung Tenormin 25mg ist momentan so in Österreich im Handel:
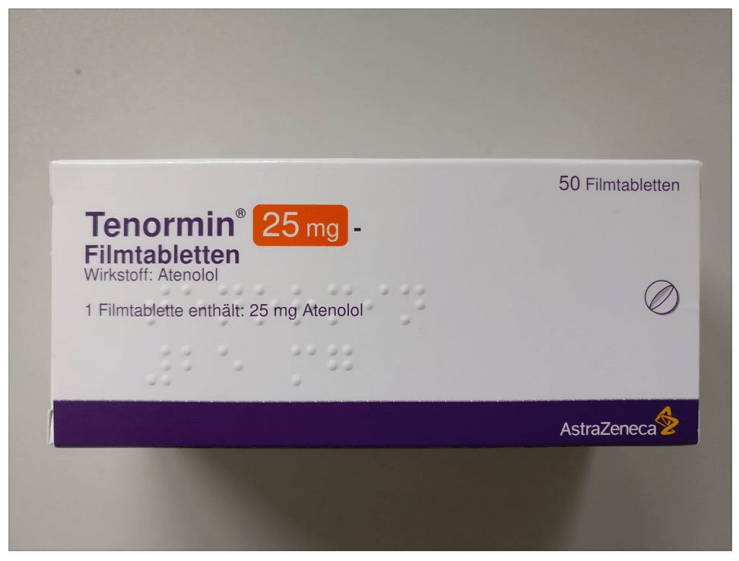
Keine Sache, oder? Ausser, dass seit einem Wechsel die Tabletten nicht mehr teilbar sind.
Da ist aber deutlich eine teilbare Tablette (mit Bruchrille) auf der Packung.
Das ist schon verschiedenen Apothekern aufgefallen und man hat bei der Firma angefragt. Die Reaktionen sind … speziell.
Das sei keine teilbare Tablette auf der Packung, sondern ein „Logo“. Alternativ: Man warte auf die Zulassung, damit man die Verpackung ändern kann.
Bis dann sind aber verschiedene Chargen im Umlauf, die optisch nicht zu unterscheiden sind. Die Firma hat einfach die unteilbaren (neuen) Tabletten in die alten Schachteln gepackt.
Sehr schön auch der Kommentar auf fb dazu von einer Kollegin, die bei der Helpline der Firma anrief um zu fragen, was der Patient, der nur eine halbe Tablette nehmen soll denn jetzt am besten macht? Anstatt Info zu geben, wie man am besten vorgeht, wird da jegliche Verantwortung abgeschoben: Sie wollen die Initialen des Patienten, wissen, welcher Arzt das verschrieben hat und das (wo?) melden, weil der Patient das geteilt nimmt und das so nicht zugelassen ist. Teilen ist/war hier nämlich nur zur erleichterten Einnahme okay, aber nicht zur Halbierung der Dosierung ….
Das erinnert mich stark an die Mitarbeiterin der Firma, bei der wir angerufen haben um nachzufragen, was die Kundin, die ihrem Familienmitglied ein in dem Land nicht erhältliches Medikament mitbringen wollte am besten tun soll. Das Problem war, dass das Medikament bis zur Anwendung gekühlt gelagert werden muss. Wir wollten anfragen, wie man das am besten handhabt (Kühlbox? versendet die Firma das vielleicht direkt?), ob das Medikament für ein paar Stunden eventuell Temperaturen über 8 Grad (vielleicht bis 20 Grad) verträgt und ob sie da Erfahrung oder Tests haben betreffend Haltbarkeit danach. Auch da kam dann alles … nur keine Antwort zu unseren Fragen. Letztendlich wurde uns noch angegeben, dass wir als Apotheke auch nach dem Verkauf des Medikamentes verantwortlich dafür seien, dass das Medikament richtig gekühlt beim Patienten (in dem Fall ein paar hundert Kilometer entfernt und im Ausland) ankommt! Danke dafür (nicht). Aber wir wissen immer noch nicht, wie das gehen soll …
Jegliche Verantwortung wird da geschickt abgelenkt. Hattet ihr auch schon solche Erfahrungen?
Nota bene: das hatten wir auch schon anders. Ich frage mich nur, ob das ein neuer Trend ist?

Wie interessant, eine Variante der „Schmuckkerbe“. Die „Einnahmehilfskerbe“ kannte ich noch nicht. Über die wahren Gründe kann man nur spekulieren. Das wird zulassungstechnische Gründe haben, die sind für den gesunden Menschenverstand nicht immer nachvollziehbar. Vielleicht hat aber auch nur einer verpennt die Artwork zu ändern und die wollen das nicht zugeben.
Bei der Transportfrage sage ich ganz klar: Ja, neuer Trend.
Die Anforderungen steigen, Stichwort GDP („Good Distribution Practices“). Da geht nichts ohne validierten Transportweg. Ich nehme an, dass sich die Mitarbeiter daher immer weniger aus dem Fenster lehnen wenn es um nicht 100% abgesicherte Dinge geht. Dazu vielleicht noch eine Prise persönliche Angst für etwas Verantwortung zu übernehmen. Und schon kommen solche Antworten heraus.
LikeLike
Ich verstehe, dass der Transportweg von einem gekühlten Medikament validiert sein soll. Nur bis wo? Nachdem es die Apotheke verlässt habe ich in keinem Fall mehr einen Einfluss darauf … ausser bei den Hauslieferungen, wo ich es vorbeibringen kann. Also: was tun? Zu sagen: tut mir leid, ich kann Ihnen das Medikament für ihre kranke Mutter nicht mitgeben, weil ich den sicheren Transport zu ihr via sie nicht garantieren kann ist auch keine Lösung.
LikeLike
Ich denke der Hersteller möchte keinerlei Empfehlungen geben wenn er keine geprüften Daten für den angefragten Fall hat. Vor 10 Jahren hätte man vielleicht noch eine Antwort bekommen in die Richtung „kann ich nicht garantieren sollte aber o.k. sein“. Inzwischen werden für alle Prozesse Daten gefordert, auch seitens der Behörden. Da lehnt sich keiner mehr aus dem Fenster:
LikeLike
Ich gebe Mr. Gaunt Recht: Vor 10 Jahren hätte man da noch die Antwort gegeben, dass das okay sein sollte, man das aber nicht garantieren könnte. Ich ergänze das noch dadurch, dass man früher auch Stabilitätsdaten rausgerückt hätte, die nicht den Eingang in ein Zulassungsdosier gefunden haben.
Das Problem ist, dass man mittlerweile sämtliche Daten aufheben muss – im Rahmen der guten Dokumentationspraxis, was an und für sich eine gute Sache ist. Paradoxerweise kann das dazu führen, dass man nur noch die Daten erhebt, die man unbedingt zwingend für die Zulassung braucht. Würde man weitere Daten erheben, könnte dabei ja ein Ergebnis rauskommen, was man selbst so nicht haben möchte. Man müsste das Ergebnis dann auch im Zulassungsdossier mit angeben. Das könnte zu einem Versagen der Zulassung führen. Das riskiert keiner, da steckt zu viel Geld drin.
Um es offen zu sagen: Den Transport eines kühlpflichtigen Medikaments in ein fremdes Land lässt sich im Rahmen der guten Distributionspraxis sauber nur über eine kontrolliert gekühlte Lieferung gewährleisten. Trans-O-Flex und Co. bieten sowas an. Wirtschaftlich ist das aber leider für eine Privatperson nicht.
Aus praktischen Gründen würde ich bei einer Autoreise eine Kühlbox empfehlen, die man an den Auto-Zigarettenanzünder anschließen kann (50 Euro) und ein Thermometer mit reinlegen. Man muss den Kunden allerdings darüber aufklären, dass die Verantwortung für diesen Transport in seinen Händen liegt.
LikeGefällt 1 Person
Vielleicht noch aus aktuellem Anlass:
Das Problem der Stabilität gibt es auch für die vielen zytostatikaherstellenden Apotheken. Es gibt viele, die Anbrüche auch nach 24 Stunden noch weiterverwenden, um Geld zu sparen. Da die Hersteller über 24 Stunden hinaus keine belastbaren Daten haben, müssen die Zytostatikaanbrüche nach Ablauf dieser Laufzeit zwingend weggeworfen werden. Viele behelfen sich da – illegalerweise – mit irgendwelchen Studien und begründen einen längeren Gebrauch damit. Falls da was passiert, möchte ich nicht der Apotheker sein, der die Freigabe genehmigt hat.
Das ist gerade im Prozess bei dem Apotheker aus Bochum interessant, der gestreckte Infusionslösungen abgegeben hat.
LikeLike
Bei dem ist noch ganz anderes schief. Echt.
LikeLike
@Pharamama: Schon klar.
LikeLike
Vielleicht noch zu dem „schon klar“ ergänzend: Man möge bitte in diesem speziellen Fall (Bochum) auch die angestellten Apotheker und PTAs gerichtlich verurteilen und diesen die Zulassung/Approbation (Apotheker) oder die Möglichkeit zur Weiterarbeit in einer öffentlichen Apotheke (PTAs) verbieten. Sie haben sich hier mit schuldig gemacht, soweit sie von diesen Praktiken wussten und das nicht gemeldet haben.
Man möge bitte auch den Apothekenrat verurteilen, der diese Praktiken überwacht und gebilligt hat, sofern er sich hier schuldhaft verhalten hat.
Just my few words…
LikeLike
Vor allem die Aufsicht – die hat da auch gewaltig geschlafen – das Bild der raffgierigen Apotheker wird dadurch nur noch weiter gefestigt…#seufz#
LikeLike
@stuttgarterapothekerin: So kam ich von diesem Blogpost auch auf den Fall Bochum. Die Amtsapothekerin hat sich so geäußert, dass ihr ein Lehrer einer PTA-Schule gemeldet hätte, dass in dieser Apotheke verfallene Anbrüche verarbeitet werden. Sie hätte ihm gesagt, dass ihr das bekannt wäre und das bundesweit so gemacht werde.
Quelle ist hier: https://www.apotheke-adhoc.de/nachrichten/detail/apothekenpraxis/pfusch-prozess-amtsapothekerin-muss-aussagen/
Die Aufsicht ist die Amtsapothekerin. Ihre Argumentation ist also, weil es jeder macht, ist es legal.
In einer anderen Quelle wird noch genannt, dass dieser PTA-Lehrer nicht nur von abgelaufenen Anbrüchen, sondern explizit von abgelaufenen Medikamenten gewarnt hätte.
Es steht auch drin, dass sie als Amtsapothekerin keine Proben gezogen hätte, da es kein Labor in Deutschland geben würde, das solche Proben untersuchen würde. Ich glaube das nicht.
Da lief auch von Seiten der Überwachung, also der Amtsapothekerin, so vieles schief…
LikeLike
@McCloud: genau das meint ich ja, diese Person sollte auch zur Rechenschaft gezogen werden….schaun mer mal
(wie ein nicht ganz unbekannter Ex-Bundestrainer mal gesagt hat – OT: von dem man schon lange nix mehr gehört hat – nach einer unsauberen Affaire ist es ziemlich still um ihn geworden, warum nur? sonst hatte er doch auch zu allem was zusagen…#grins#)
LikeLike
Andererseits hat es bis zu einem Gerichtsurteil gedauert, bis eine Krankenkasse lernen musste, dass, nur weil es Studien für die Lagerung unter bestimmten Parametern in z.b. einer großen Klinikapotheke gibt, dies noch lange nicht auf alle Apotheken umzulegen ist. (Die Kasse hatte die Zulässigkeit der abgerechneten Verwürfe bezweifelt, „weil es ja Studien gibt“ und die Vorschriften zur Abrechnung, die sich aus der Hilfstaxe ergeben, schlichtweg ignoriert) (Und wehe, man hat mal was entsorgt, weil bei 24 Stunden Haltbarkeit für den nächsten Tag kein Patient geplant war und dann – 23 Stunden und 58 Minuten nach der letzten Herstellung doch noch eine Herstellung gemacht werden musste… Bezahlt ja auch keine KK)
Und nein! Das soll keine Verteidigung für den Bochumer Apotheker sein!
LikeLike
@Desiree: Ich habe so den Eindruck, dass man sich diese Studien wild aus dem Internet zusammenkopiert.
Eine Pharmafirma prüft ein Medikament in ihrer In-Use-Spezifikation auf etwa 15-25 verschiedene Punkte. Dazu braucht man mindestens schon mal eine HPLC, die eine zytostatikaproduzierende Apotheke nicht hat. Die auftretenden Zerfallsprodukte muss man strukturell chemisch aufklären, dazu braucht man eine GC und/oder andere kostspielige Geräte. Anschließend muss man nachweisen, dass diese chemischen Zerfallsprodukte in diesen Dosen nicht toxisch sind. Dazu kommen noch Keimbelastungskontrollen (TAMC, TYMC, Abwesenheit von E.Coli) und andere Nachweise.
Ich bezweifle stark, dass in den „Studien“ aus dem Internet die komplette Spezifikation geprüft wird, zumal diese vertraulich ist. Irgendein einsam arbeitender Doktorand hat also beispielsweise an der Uni HongKong zwei bis drei dieser etwa 20 Punkte geprüft und dabei noch ein paar Daten gehübscht, damit das Ergebnis nach seinen Wünschen ist. Und darauf baut dann ein deutscher zytostatikaproduzierender Apotheker seine Argumentation auf, dass seine Zytostatikaverwürfe länger haltbar wären.
Will sagen: Auch eine „große Krankenhausapotheke“ hat weder die Geräte noch die finanziellen Mittel um derartige Studien durchzuführen.
LikeLike
Hmm…. Den Hinweis, dass eine Bruchkerbe nicht zum dosisgleichen teilen, sondern nur zur Schluckerleichterung ist, findet man in der deutschen Datenbank öfters. Gewöhnlicher Weise ist dann aber auch unter „Teilbarkeit“ ein „-“ eingetragen, im Gegensatz zu z.B. „1/2“ für halbierbar.
Dass eine Herstellerfirma mal eben aber die Produktion umstellt und die Packungen dann „falsch“ beschriftet ist natürlich Mist. Erinnert mich aber etwas an „Amlodipin Dexel 5mg*-Tabletten, die früher mal halbierbar waren, und mit der Umstellung der Rabattverträge der „großen grünen Krankenkassen“ plötzlich nicht mehr halbierwar waren (angeblich, weil die Kassen das so in die Ausschreibung geschrieben hatten). Führte mehrfach zu Verwirrung – und immer wieder zu Problemen…
Auch lustig der Zwangsaustausch bei „Allopurinol 300mg“ auf die Firma, die sich 1/3eln läßt. Wenn der Arzt dann mal wieder NICHT die Dosierung (1x tgl. 1/2) auf das Rezept vermerkt hat, und der Patient Wochen später die Packung umtauschen will, weil er die ja nicht halbieren kann…
Aber der Versandhandel mit Arzneimitteln aus dem Ausland wird das alles richten. Da ist nämlich die Retourenbeschwerde so kompliziert, dass man als Patient halt mit dem lebt, was man bekommen hat… Und so ist es doch von Politik und kassen gewollt – wir sparen uns alle zu Tode.
LikeLike
Der letzte Absatz ist so wahr.
LikeLike
Äh… mal blöd als Laie gefragt…
Was ist denn die Alternative, die dem Hersteller vorschwebt? Gibt es GANZE Tabletten mit der halben Wirkstoffmenge derer, die der Arzt verschrieben hat?
LikeGefällt 1 Person
Nö. (Also hier jedenfalls nicht)ö. Aber das interessiert den Hersteller nicht mehr.
LikeLike
Okay… also wenn zur Blutdruckregulierung der Person nur die halbe Wirkstoffmenge einer von der Firma hergestellten Tablette benötigt wird, dann will der Hersteller den Arzt und Patienten „melden“? Den Patienten als Apostat, weil sich dessen Blutdruck nicht an die Vorgaben der Pharmaindustrie hält und den Arzt, weil der solches abweichlerisches Verhalten auch noch unterstützt?
LikeLike
Nicht wirklich hilfreich, oder? 😬
Du erkennst den Wahnsinn heute …
LikeLike
Nun ja, das „nicht an die Vorgaben der Pharmaindustrie hält“ ist nicht so einfach.
Medikamente werden zugelassen, und das für jede Dosierung. Bzw. bei offizieller (!) Teilbarkeit der Tabletten muss sichergestellt sein, dass diese auch innerhalb bestimmter Grenzen zuverlässig teilbar sind. Das fordert der Gesetzgeber. Es könnte gut sein dass Tenormin Probleme mit der Zulassungsbehörde wg. der Bruchkerbe bekommen hat. Diese suggeriert sichere Teilbarkeit für halbe Dosis, das ist aber so nicht vorgesehen.
Auch andere Atenolol-Präparate fangen bei 25mg an. Für hohen Blutdruck sind 50mg oder 100mg Dosierung übliche Erhaltungsdosis. Da könnte man dann noch das Finetuning mit 25mg machen. Eine 12,5mg Dosierung ist offenbar nicht vorgesehen.
LikeLike
Zumindest in der BRD gibts Generika, die halbierbar sind…wie das in Ch bzw A aussieht, keine Ahnung.
LikeLike
Kleine Info aus Österreich:
„Eine 12,5mg Dosierung ist offenbar nicht vorgesehen.“ – naja… zumindest in der österreichischen Fachinfo steht:
*Patienten mit eingeschränkter Nierenfunktion:
Da Atenolol über die Nieren ausgeschieden wird, ist die Dosierung im Falle einer schweren Niereninsuffizienz anzupassen.
GFR (ml/min/1,73 m2 KOF) Dosierung
LikeLike
Mein Lieblingsproblem war ein Antipsychotikum, bei dem die Absetzung geplant war. Dosis bisher 1 mg/Tag. Antipsychotikum bedeutet: Ausschleichen. Problem: 1 mg ist von allen Herstellern die kleinste Stärke, die Hälfte hat davon Kerben, aber KEINE EINZIGE ist teilbar. Nach Rücksprache mit den Herstellern: Jop, Teilbarkeit ist nicht zugelassen, daher nicht erlaubt. Super!
Arzt hat sich dann für 1 mg alle 2 Tage entschieden…finde ich auch nicht so super, aber was soll man machen
LikeLike
ich hatte mal ein Antidepressivum, bei dessen Absetzung ich abartige Absetzerscheinungen bekam. die Dosierung war so grob, dass ich zum Ausschleichen die Kügelchen in der Kapsel zählen, ein paar Kügelchen wegnehmen und die Kapsel wieder zusammenbauen musste. das hat einen knappen Tag pro Woche gedauert.
LikeLike
Ergänzung: ein teilbares Präparat eines anderen Herstellers war aufgrund des Rabattvertrags nicht drin.
LikeLike
Also ich habe im Kompendium spontan 3 Atenolol-Generika gefunden, die allesamt Bruchrillen bei den 25mg-Tabletten haben. Die werden doch nicht auch etwa nicht zu teilen sein?
LikeLike
Da will halt keiner Aussagen abgeben, für die er am Ende die Verantwortung tragen muss.
Ich wollte von einer Firma, die Polypektomie-Klammern herstellt, mal wissen, ob ein bestimmtes, genau bezeichnetes Produkt, das in meinem Dickdarm steckt, MRT-fähig ist. Es war glasklar, um welches Produkt es ging, aber man wollte mir keine Auskunft geben, weil ich kein medizinisches Fachpersonal bin.
Völliger Schwachsinn.
Ende vom Lied war dann, dass meine Cousine, die Ärztin ist, angerufen hat. Der konnte dann mitgeteilt werden, dass das Produkt nicht MRT-fähig ist.
LikeLike